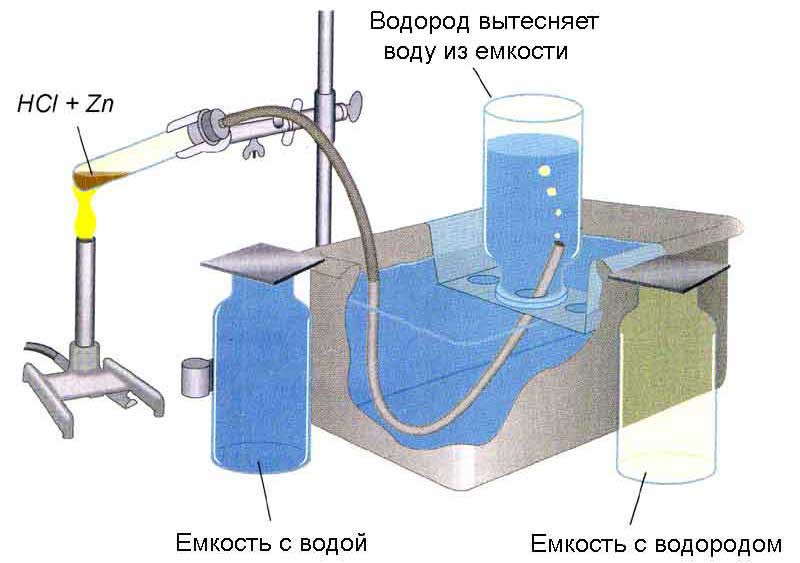
Сколько же нам удалось получить водорода?
Допустим, мы сделали электролизер, блок питания, соединили все вместе и наслаждаемся бульканьем газа. Теперь самое время определить сколько газа мы можем получить.
Казалось бы
простое дело. Химики это делают постоянно. Установка простая и мы помним ее, еще
со школы.
Одна, только, проблемка. В перевернутой емкости кроме газа, объем которого мы измеряем, присутствуют пары воды. Сколько их там? Вы будете удивлены, но их там немало.
Для пересчета объемов
газов и паров воды необходимо знать только закон Дальтона, который говорит, что
«давление смеси газов состоит из суммы парциальных давлений его компонентов». В
нашем случае, общее давление состоит из давления водорода, кислорода и паров
воды, то есть: P = P(H2) + P(O2) + P(H2O). Общее давление равно
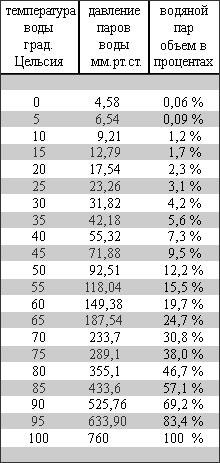
атмосферному, то есть 760 мм.рт.ст., а давление паров воды возьмем из таблицы. Продолжение таблицы - здесь, расширеная таблица - здесь.
Дальше – проще:
Допустим, что температура 25 градусов Цельсия. Тогда давление кислорода и водорода будет меньше атмосферного на величину давления паров воды.
P(H2) + P(O2) = P – P(H2O) = 760 мм.рт.ст. – 23,26 мм.рт.ст. = 736,74 мм.рт.ст.
Переведем давление в атмосферы.
760 мм.рт.ст. = 1 атм.,
736,74 мм.рт.ст. = х = 0,97 атм.
Если пропустить уравнение состояния идеального газа, то результат 0,97 говорит о том, что водород с кислородом будут занимать 97 процентов объема, а оставшиеся 3 процента займут пары воды.
Что бы не мучаться с расчетами каждый раз, я добавил в таблицу дополнительную колонку, где пересчитано содержание водяного пара при атмосферном давлении.
Содержимое таблицы нужно читать так: «в смеси любых газов при температуре "50" градусов Цельсия есть место для "12,2%" воды в газообразном состоянии».
Вода, в газообразном состоянии, такой же газ, как кислород и водород. Единственное отличие в том, что она может конденсироваться, то есть переходить из газообразного состояния в жидкое.
Ради чего это все?
Часто приходится рассматривать конструкции электролизеров с точки зрения производительности по кислороду и водороду, в зависимости от тока и напряжения. Или сравнить свой электролизер с уже существующим. Единственный быстрый способ это сделать – собрать выделившийся газ в литровую бутылку и измерить время за которое она наполнится. После этого посчитать мощность, перемножив ток на напряжение на электролизере. В результате получим количество газа в минуту, в зависимости от мощности. Вроде все просто, но проблема заключается в том, что вместе с кислородом и водородом, из электролизера, выходит водяной пар. При 40 градусах Цельсия его 7%, а при 90 – 70% (по объему).
Именно этим трюком пользуются продавцы электролизеров, которые показывают немыслимую производительность продаваемых изделий. К примеру, разогрев электролизера до 80 градусов Цельсия удваивает производительность за счет водяного пара, а при 96 - удесятеряет!
Им помогает то, что «ячейка Мэера вырабатывающая газ Брауна» - это чисто журналистское понятие. Ячейка Мэера плохо повторяема, а газ Брауна не имеет четкого химического состава.
Но есть и положительный момент, который заключается в том, что мы можем менять отношение " водяной пар - кислород-водород " изменяя температуру электролизера.
Если Вы знаете, как будет себя вести водяной пар при изменении температуры и давления, то дальше можно не читать.
Допустим, мы собрались подавать смесь водорода, кислорода и водяного пара в двигатель. Как он себя будет вести? Совершенно не хотелось бы, что бы пар превратился в жидкость и испортил двигатель.
При понижении температуры пар начинает конденсироваться, это понятно. А при повышении давления? Для того что бы ответить на последний вопрос достаточно перевести таблицу в графическую форму (красная линия показывает момент закипания воды в зависимости от температуры и давления).
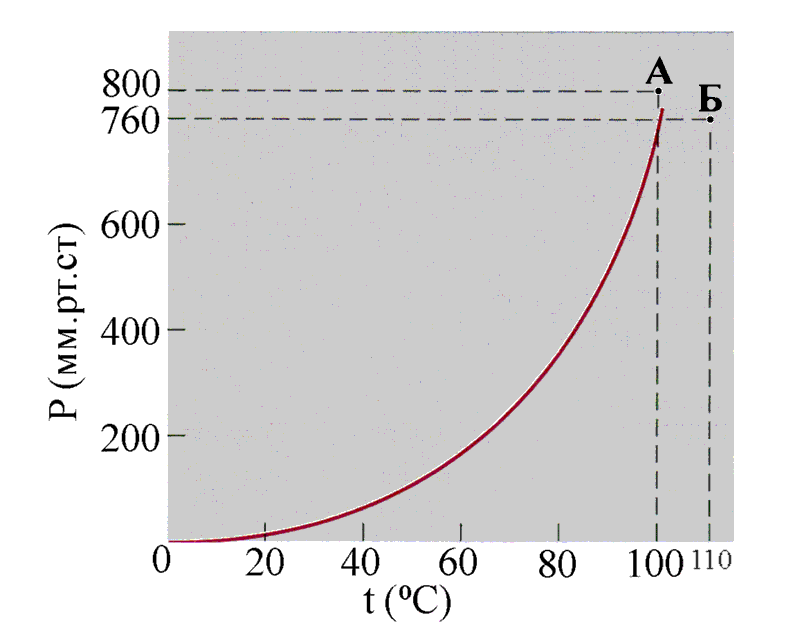
Мы знаем, что вода начинает кипеть при 100 гр.Цельсия и давлении 760 мм.рт.ст. Тогда можно предположить, что при 100 гр.Цельсия и большем давлении, к примеру 800 мм.рт.ст. она кипеть еще не будет. Логично? Это точка «А». Предположим, что при давлении 760 мм.рт.ст. мы увеличиваем температуру до 110 гр.Цельсия. Конечно. Вода закипит и, скорее всего, выкипит вся. Это точка «Б». Теперь, весьма логично будет предположить, что красная линия разделяет воду в жидком и газообразном состоянии. То есть, при условиях левой части графика – вода может находится в жидком состоянии, а справа – только в газообразном.
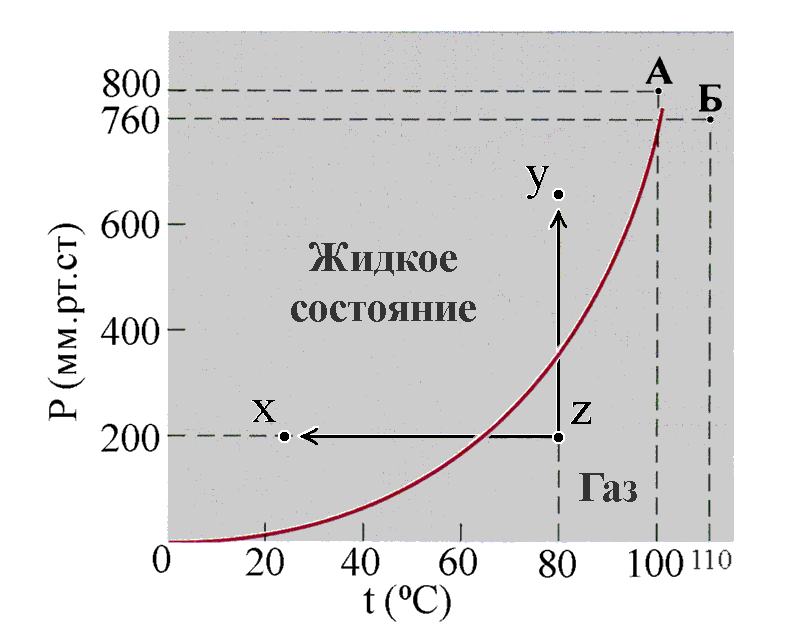
А теперь возьмем какую-нибудь точку «Z» при высокой температуре и низком давлении, когда вода, наверняка, будет находится в газообразном состоянии. Пусть это будет 80 град. Цельсия и 200 мм.рт.ст. Теперь, охладив водяной пар при постоянном давлении 200 мм.рт.ст., мы перейдем в точку «X». При этом водяной пар должен начать конденсироваться и превращаться в воду. Увеличив давление при постоянной температуре 80 град.Цельсия, мы перейдем в точку «Y», что приведет к аналогичному результату.
Вывод. Водяной пар будет конденсироваться при понижении температуры и повышении давления.
Практический результат следующий. Какой бы насыщенный пар мы бы не подавали в двигатель это никогда не приведет к конденсации воды, так как в воздушном коллекторе пониженное давление и повышенная температура.
Это, конечно, не самое точное объяснение, но за то, мы обошлись без формул, изохор, изотерм и адиабат : )
Значительно бо'льшую опасность для двигателя представляют пары электролита, которые неизбежно выносятся из электролизера вместе с парами воды. Они «сжирают» алюминиевые детали. Коррозия продолжается даже когда двигатель выключен. Стальным и чугунным деталям, то же достается. О том как этого не допустить и быстро проверить газ на выходе электролизера – читайте дальше.
_